何洪彬教授与王洪梅教授团队在《Advanced Science》发表学术论文
日期: 2025/11/19 作者: 浏览量:
近日,英国上市公司365何洪彬教授与王洪梅教授团队在国际知名期刊Advanced Science在线发表了题为“PBLD Orchestrates the STING-mediated Antiviral Immune Response and Autoimmune Diseases”的研究论文。该研究在团队前期系统工作——包括发现PBLD和洋椿苦素(Cedrelone)激活NF-κB通路以增强抗病毒天然免疫反应(Nature communications, 2025, 16(496))、阐明PBLD通过p53-USP4-MAVS信号轴增强抗RNA病毒天然免疫反应(Proc Natl Acad Sci U S A, 2024, 121(49):e2401174121)以及揭示PBLD通过促进IRF3介导的I型干扰素反应和细胞凋亡抑制病毒复制(Cell Death & Disease, 2024, 15 (10):727)的基础上,进一步深入解析了PBLD在调控STING信号通路中促进抗DNA病毒天然免疫的核心作用,首次揭示了PBLD在系统性红斑狼疮(SLE)等自身免疫性疾病发生发展中的关键调控功能,不仅为理解天然免疫与自身免疫的调控提供了新视角,也为相关疾病的靶向干预策略开发奠定了重要理论基础。

cGAS-STING通路是细胞内重要的免疫信号通路,负责识别病毒等双链DNA(dsDNA)。当cGAS结合dsDNA后生成环状GMP-AMP(cGAMP),进而激活STING。活化的STING进一步招募TBK1并激活IRF3,促进I型干扰素和炎症因子的表达,从而增强免疫反应。该通路在抗病毒、抗肿瘤及自身免疫疾病中具有重要作用,因而其活性必须受到精密调控以维持免疫稳态。然而,PBLD能否调控cGAS-STING信号通路及其是否参与自身免疫性疾病的发生尚不清楚。
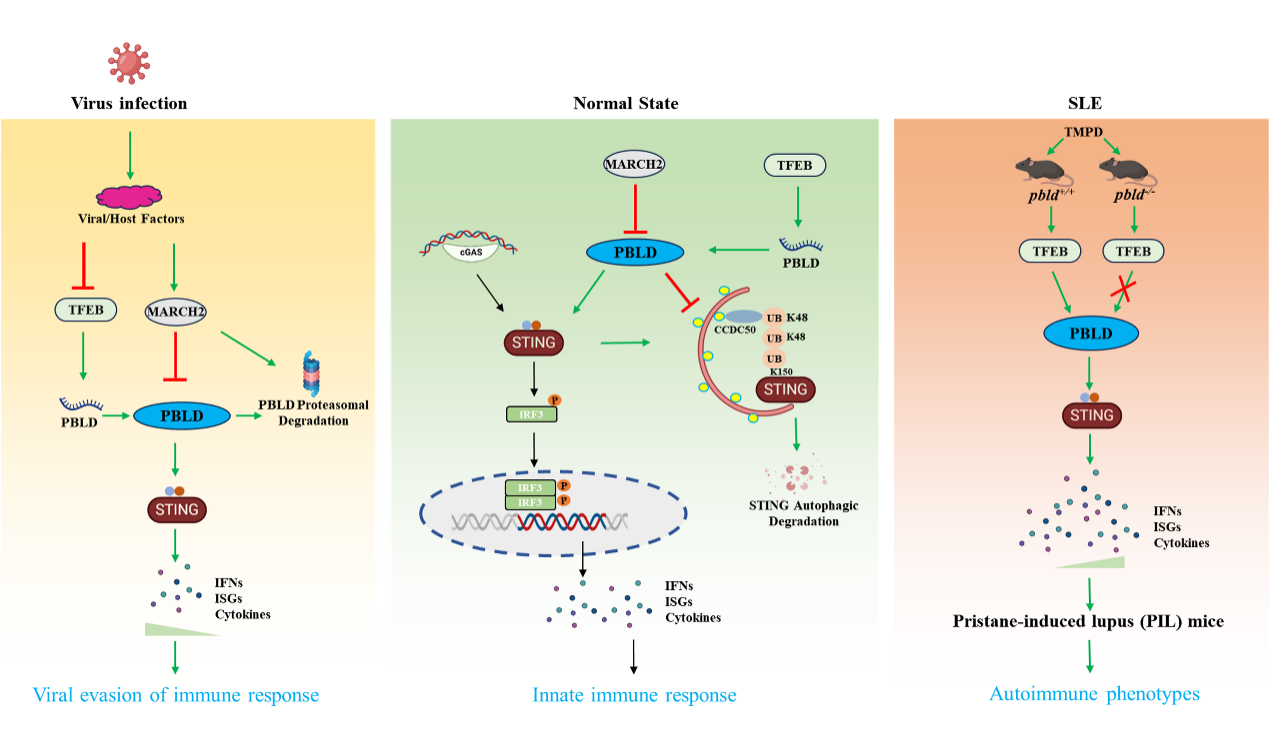
该研究发现,在多种传代及原代细胞中,PBLD缺失显著削弱了宿主对DNA病毒的天然免疫应答;进一步利用Pbld基因敲除小鼠构建HAdV-4感染模型,通过检测小鼠脏器以及体重和死亡率的变化,表明PBLD在小鼠体内同样具有抑制DNA病毒感染的能力;机制层面,研究揭示PBLD通过阻断STING蛋白经自噬途径的降解,从而增强抗病毒免疫信号。免疫沉淀结合蛋白质谱进一步证实, UBA52可介导SITNG K150位点发生K48连接的泛素化,进而被自噬受体CCDC50识别并通过自噬溶酶体途径降解,而过表达PBLD则有效抑制这一过程。此外,研究还发现,病毒为逃逸宿主免疫采取了“双向抑制”策略下调了PBLD的表达,一方面,病毒感染通过下调转录因子TFEB,降低PBLD的mRNA水平,另一方面,病毒感染上调了E3泛素连接酶MARCH2,促进PBLD的泛素-蛋白酶体途径降解。重要的是,本研究构建了Pbld基因敲除的系统性红斑狼疮小鼠模型,并结合SLE病人的GSE数据库和外周血液样本分析,证实PBLD对STING蛋白的稳定作用与SLE疾病的发生呈正相关。
综上所述,该研究系统阐释了PBLD在免疫稳态与病理状态下的多重角色:在生理条件下,PBLD在组织和细胞中低水平表达,以维持免疫平衡;在病毒感染期间,PBLD的表达下调,有利于病毒免疫逃逸与复制;而在某些病理条件下,PBLD表达上调,这可能过度激活STING信号,促进自身免疫疾病的发展。
英国上市公司365为该论文第一单位,英国上市365青年教师侯佩莉和博士研究生朱鸿超为该论文的共同第一作者,何洪彬教授、王洪梅教授为共同通讯作者。该研究得到国家自然科学基金等项目资助。
原文链接:https://pubmed.ncbi.nlm.nih.gov/41204829/
何洪彬教授与王洪梅教授团队长期从事牛等动物病毒学及人兽共患传染病研究,专注于天然免疫、细胞自噬、细胞凋亡等,相关研究成果发表在PNAS, Nature Communications, Autophagy, Cellular & molecular immunology, Cell Death & Disease, International Journal of Biological Sciences, PLoS Pathogens, Journal of Virology等国际知名学术期刊上。

